刘涛《常见的酸和碱》交流型课堂复习课教学设计
《常见的酸和碱》复习课教学设计
西安市阎良区西飞第一中学 刘涛
一、教学内容分析:
《常见的酸和碱》是九年级化学下册重要内容,酸碱部分的知识因其知识点多,知识点之间的联系紧密而成为初中化学教学中的重难点,酸碱的化学性质是中考命题的必考考点。学生在做酸碱题目时,不懂得利用酸碱的性质规律分析题目,所以这节常见酸、碱的复习课帮助学生梳理酸碱部分的知识点,加强知识点之间的联系;然后通过交流案的典例分析,引导学生在解题时能将酸碱的化学性质应用在解题中。在解题时有一个较为清晰的思维过程,培养了学生的思维能力和解题能力。
1、 教学目标:
(1)知识与技能:
①知道常见酸的特性、用途及酸的稀释方法
②知道常见酸和碱的主要性质和用途。
③掌握酸、碱的化学性质
(2)过程与方法:
通过总结酸碱的化学性质,培养学生归纳总结的能力和学习方法,培养学生解决实际问题的能力。
(3)情感态度与价值观:
培养学生自主探索发现的好奇心和探究欲。培养学生的合作意识,以及勤于思考、严谨求实、勇于创新的科学精神。
2、教学重点:酸、碱的化学性质及应用
难点:归纳总结酸、碱的化学性质
3、学情分析:
本班学生基础比较好,大部分同学已掌握,但知识灵活运用能力较差。他们还没有形成知识体系,缺乏知识的整合能力及将知识运用于实践的能力。根据学生这一特点,复习时重基础,适当拓展。
4、教学方法:《常见酸和碱》交流案、PPT、微课视频,合作交流,问题探究法、讨论归纳等
二、教学活动过程:
(一)创设情境 导入复习
趣味情景导入:展示人被蚊虫叮咬后,会感到痛痒,如果立即用肥皂水等物质涂在叮咬处,就会感到痛痒减轻,你知道其中的道理吗?
设计意图:吸引学生的注意力,激起学生学习的兴趣与热情。
(二)课程流程
1、展示考试内容和要求:
(1)知道常见酸的特性、用途及酸的稀释方法。(必考)
(2)知道常见碱的特性、用途。(必考)
(3)掌握酸、碱的化学性质。(必考)
展示意图:让学生明确本节课学习的内容和要求,每一点后面备注(必考),引起学生的高度重视。
2、回顾知识习题与复习要点
(1)常见的酸
【回顾知识习题】
例1、实验室有两瓶失去标签的无色液体,体积都是500mL。老师告诉小明:其中一瓶是浓盐酸,一瓶是浓硫酸,并请小明帮忙为它们重新贴上标签,小明很快就完成了。你想,小明可能用什么方法区分开二者的?
设计意图:发散学生的思维,学生可以通过多种方法区别两种无色溶液,培养学生多角度分析问题的能力。
【复习要点】1、浓盐酸、浓硫酸的性质
颜色 | 状态 | 气味 | 打开瓶盖的现象 | 特性 | 在空气中长期敞口放置后的变化 | |
浓盐酸 | 无色 | 液体 | 刺激性气味 | 白雾 | 挥发性 | 溶质质量分数 减小 |
浓硫酸 | 无色 | 黏稠、油状 | 无味 | 无现象 | 吸水性、 脱水性、 腐蚀性 | 溶质质量分数 减小 |
【请一位同学展示关于浓盐酸、浓硫酸相关性质】
【提出问题】浓盐酸易挥发、浓硫酸具有吸水性,故如何保存?
【学生回答】密封保存。
 【提出问题】实验室中常用到稀盐酸、稀硫酸,那么如何将浓硫酸稀释为稀硫酸呢?
【提出问题】实验室中常用到稀盐酸、稀硫酸,那么如何将浓硫酸稀释为稀硫酸呢?
【学生回答】酸入水、沿器壁,慢慢倒、不断搅
【回顾知识习题】
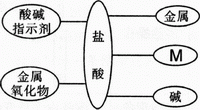
例2、(2010年陕西中考)构建知识网络,可以帮助我们理解知识间的内在联系。右图是盐酸与不同类别物质之间反应的知识网络。
(1)图中M应为 盐 类物质。
(2)写出一种能与盐酸反应的金属镁(锌、铁)。
(3)盐酸能与碱反应的实质是盐酸中的 H+ (写离子符号)与碱中的 OH-反应生成H2O。
(4)用盐酸除铁锈(主要成分Fe2O3)的化学方程式
是Fe2O3+6HCl=2FeCl3+3H2O
【复习要点】2、酸的化学性质(通性)和用途
(1)酸具有通性的原因
酸溶液中都含有氢离子(或H+),因此酸具有相似的化学性质。
酸的通性
酸的化学性质 | 反应的化学方程式 | 实验现象 |
酸与指示剂的反应 | 酸使紫色石蕊溶液变红;使无色酚酞溶液不变色 | |
酸与活波金属的反应 | 镁与稀盐酸、稀硫酸 | 有气泡产生 |
锌与稀盐酸、稀硫酸 | 有气泡产生 | |
铁与稀盐酸、稀硫酸 | 有产气泡生,溶液由无色变为浅绿色。 | |
酸与金属氧化物反应 | 氧化铁与稀盐酸、稀硫酸 | 红色粉末逐渐消失,溶液由无色变为黄色。 |
氧化铜与稀盐酸、稀硫酸 | 黑色粉末逐渐消失,溶液由黑色变为蓝色。 | |
酸与碱的反应 | 氢氧化钠与稀盐酸、稀硫酸 | 反应无现象 |
氢氧化钙与稀盐酸、稀硫酸 | ||
与盐的反应 | 碳酸钙、碳酸钠与稀盐酸 | 有气泡产生 |
硝酸银溶液和稀盐酸 氯化钡溶液与稀硫酸 | 生成白色沉淀 |
【学生活动】小组合作完成,重点的化学方程式学生板演。
 【教师点拨】重点化学方程式的应用以及使用时的注意事项。
【教师点拨】重点化学方程式的应用以及使用时的注意事项。
(二)常见的碱
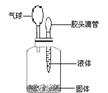
【回顾知识习题】例3、要使右图装置中的小气球鼓起来,实验时使用的固体和液体应该是( A )
①镁和稀盐酸 ②石灰石和盐酸 ③氯化钠和水
④氢氧化钠和水⑤生石灰和水 ⑥硝酸铵和水
①②④⑤B.①②③⑤
C.①②④⑥D.①③④⑤
【学生活动】4人一组讨论1分钟、小组交流、1-2位同学展示。
【方法点拨】教师提前录制好关于本题的微课教学视频,时间2分钟,学生展示结束后播放。
【设计意图】培养学生的合作意识、探究意识,分析问题,归纳总结的能力。
【复习要点】
1、氢氧化钠、氢氧化钙的物理性质
氢氧化钠NaOH | 氢氧化钙Ca(OH)2 | |
俗称 | 火碱、烧碱、苛性钠 | 熟石灰、消石灰 |
色态 | 白色固体 | 白色固体 |
溶解性 | 易溶于水,并放出大量的热 | 微溶于水 |
特性 | 氢氧化钠固体易吸收空气中的水分而潮解 | 溶解度随温度的升高而减小 |
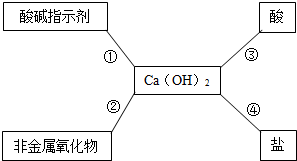 【回顾知识习题】例4、如图是有关氢氧化钙的知识网络。
【回顾知识习题】例4、如图是有关氢氧化钙的知识网络。
(1)遇氢氧化钙溶液变红的酸碱指示剂
是无色酚酞溶液。
(2)若图中非金属氧化物为CO2,
则反应②的化学方程式CO2+Ca(OH)2=CaCO3↓+H2O。
(3)反应③在生产中的一种用途是中和酸性土壤。
(4)有反应④制取NaOH所用到的盐是Na2CO3,发生反应的化学方程式为Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
【复习要点】2、碱的化学性质
(1)碱具有通性的原因
碱溶液中都含有氢氧根离子(或OH-),所以它们具有相似的化学性质。
碱的化学性质(或通性)
碱的化学性质 | 反应的方程式 | 实验现象 |
碱与指示剂的反应 | 碱使紫色石蕊溶液变蓝; 使无色酚酞溶液红 | |
碱与非金属氧化物的反应 | 氢氧化钠溶液与二氧化碳 | 无现象 |
氢氧化钙溶液与二氧化碳 | 澄清石灰水变浑浊。 | |
碱与酸的反应 | 氢氧化钠溶液与盐酸 | 无现象 |
碱与盐的反应 | 氢氧化钠溶液与硫酸铜溶液 | 产生蓝色沉淀 |
氢氧化钠溶液与氯化铁溶液 | 产生红褐色沉淀 | |
氢氧化钙溶液与碳酸钠溶液 | 产生白色沉淀 |
【学生活动】小组合作完成,重点的化学方程式学生板演。
【教师点拨】重点化学方程式的应用以及使用时的注意事项。
3、中考命题趋势,例题讲解。
【命题点一】常见的酸
例1、(2015·湖北黄冈)构建模型和构建知识网络是化学学习中重要的学习方法,李华同学利用左手构建酸的性质知识网络,如图所示,请结合图示回答下列问题:
(1)如用湿润的pH试纸测定盐酸的pH,则结果会偏小(填“偏大”“偏小”或“无影响”)。
(2)图中①的现溶液变红。
(3)写出一个符合图中③的化学式: HCl+AgNO3=AgCl↓+HNO3
(4)图中性质④属于复分解反应(填基本反应类型)。
(5)图中⑤的性质在工业上可用于除铁锈(填用途)。
【方法点拨】教师利用录制的微课《五指法记忆酸的化学性质》,帮助学生进一步落实基础知识。
【命题点二】 常见的碱
 例2、(2013年陕西)许多化学反应都伴随着明显的现象。但也有一些观察不到明显现象。请回答下列问题:
例2、(2013年陕西)许多化学反应都伴随着明显的现象。但也有一些观察不到明显现象。请回答下列问题:
(1)向FeCl3溶液中滴加NaOH溶液,出现的明显现象产生红褐色沉淀
(2)盐酸与NaOH溶液的中和反应也无明显现象,为证明二者确实发生了化学反应,在向NaOH溶液中滴加盐酸前,应先向NaOH溶液中滴入少许无色酚酞试液。
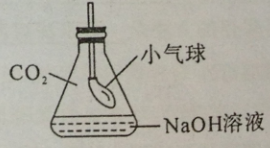
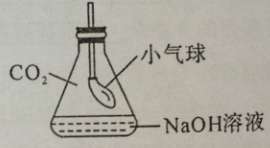
(3)CO2与NaOH溶液的反应无明显现象。为证明二者发生了反应,小红同学设计了如右图所示的实验。向一盛满CO2气体的锥形瓶中注入一定量的NaOH溶液,迅速塞紧橡皮塞(胶塞中插有一下端系小气球的玻璃管)。然后振荡锥形瓶,
会观察到小气球逐渐胀大,其主要原因是二氧化碳与氢氧化钠发生反应,
使锥形瓶内压强减小。
【知识拓展】 探究二氧化碳与氢氧化钠溶液反应
1、原理:CO2+2NaOH====Na2CO3+H2O
2、验证氢氧化钠是否和二氧化碳反应的思路
(1)可以利用密闭的装置,根据氢氧化钠和二氧化碳反应后会导致密闭容器中压强减小,从而引起现象的变化而判定。
思路判断时常出现的问题:氢氧化钠溶液中含有水,二氧化碳也能和水发生反应,必须设计对比实验排除水对实验结果的影响。
【学生活动】学生观看微视频,了解验证氢氧化钠是否和二氧化碳反应的思路。
(2)可以利用反应后的产物为碳酸钠(同学们,请写出你的方法)
方法 | 现象 | 反应原理 |
加入过量的稀盐酸 | 有气泡产生 | Na2CO3+2HCl=2NaCl+CO2↑+H2O |
加入澄清的石灰水 | 有沉淀产生 | Na2CO3+Ca(OH)2=2NaOH+CaCO3↓ |
加入氯化钡或氯化钙溶液等 | 有沉淀产生 | Na2CO3+BaCl2=2NaCl+BaCO3 ↓ |
【学生活动】观看关于碳酸钠的微课视频,复习回顾碳酸钠的相关化学性质。4人一组讨论交流。3-5位同学展示分享小组的结构。
【教师点评】以上几位同学都是利用检验生成物碳酸钠来验证二氧化碳与氢氧化钠的反应,
归纳总结。同学们本节课你学到了什么?与大家分析。
课堂检测:
一次,小刚在实验室看到了右图情景:
他首先想到药品可能变质了,那么NaOH
溶液在空气中变质的化学方程式
为2NaOH + CO2 = Na2CO3 + H2O;
小刚利用实验室的三种试剂(氯化钙溶液、稀盐酸、酚酞试剂)对这瓶“NaOH溶液”展开了探究。
[提出猜想]猜想①:氢氧化钠溶液没有变质 猜想②:氢氧化钠溶液部分变质
猜想③:氢氧化钠溶液完全变质
[实验探究]
方案 | 现象 | 结论 | |
1 | 取少量溶液于试管中,滴入足量盐酸试剂 | 产生大量气泡 | 猜想①不成 |
2 | 取少量溶液于试管中,滴加酚酞试剂 | 溶液变红 | 溶液中一定含有NaOH |
3 | a.取少量溶液于试管中,滴加足量CaCl2试剂 | 产生白色 沉淀 | 猜想②成立 |
b.向a中所得溶液中滴加酚酞 | 溶液变红 | ||
经过思考,小刚否定了方案2的结论,理由是Na2CO3溶液也能使酚酞变红。
[反思评价]氢氧化钠溶液暴露在空气中容易变质,故应密封保存。
(四)作业设计:复习资料上的相关习题。
(五)板书设计:
浓盐酸 氢氧化钠
浓硫酸 氢氧化钙
金属 指示剂
酸 碱 非金属氧化物
金属氧化物 盐
用途 用途
教学反思:
本节课首先将本专题在中考中的要求和内容给学生呈现出来,让学生了解本节课的重要性,带着任务去学习。其次,通过典例分析(选取的例题都是历届陕西省的中考题)---归纳总结(让学生通过中考题总结归纳),同时借助思维导图、表格等提供小结,形式多样。通过学生的自主参与,零碎的知识按照不同方式搭起了骨架,有了主线,有了精髓,基本概念和基本原理在学生脑海中扩大、加深,这就使学生应用概念解决新问题的能力得到了加强。同时对常见的酸和碱的命题趋势通过典型例题进行展示。本节课也重视知识的迁移性训练,通过解决一系列实际生活中与酸和碱相关问题以达到举一反三、触类旁通的教学效果。最后,本节课将初中化学交流案、PPT、微视频等教学资源有机得结合起来中充分利用交流案,节省了教学的时间。顺利地完成了本节课的教学任务。体现科学思想和科学方法,贯穿了交流的思想,体现了交流型课堂的特色,采取的教学方法灵活多样,体现了师生、生生、生本间的知识知识和情感的交流。具体表现在“读”、“议”、“探”、“展”、“练”,以议为铺垫,关注合作交流。以展为核心,关注表达展示。以探为重点,关注科学探究的方法。以练为保证,重视巩固应用,课堂上大胆尝试微课辅助教学,效果较好。整节课学生活动多,知识容量较大,能形成知识网络帮助学生记忆和了解。但是也有许多不足的地方,如:关于酸和碱的性质有个实验让学生体验,趣味性更强;微课制作更加的精美一些,更利于学生观看,提高其注意力。
专题 常见的酸和碱交流案
姓名: 班级: 学校:西飞一中高新合作部 时间:3月16日
一、考试内容和要求:
1、知道常见酸的特性、用途及酸的稀释方法。(必考)
2、知道常见碱的特性、用途。(必考)
3、掌握酸、碱的化学性质。(必考)
二、回顾知识习题与复习要点
(一)常见的酸
【回顾知识习题】例1、实验室有两瓶失去标签的无色液体,体积都是500mL。老师告诉小明:其中一瓶是浓盐酸,一瓶是浓硫酸,并请小明帮忙为它们重新贴上标签,小明很快就完成了。你想,小明可能用什么方法区分开二者的?
【复习要点】1、浓盐酸、浓硫酸的性质
颜色 | 状态 | 气味 | 打开瓶盖的现象 | 特性 | 在空气中长期敞口放置后的变化 | |
浓盐酸 | 无色 | 液体 | _______ | ________ | ________ | 溶质质量分数_____ |
浓硫酸 | 无色 | 黏稠、油状 | 无味 | 无现象 | ________、________、________、 | 溶质质量分数_____ |
【回顾知识习题】例2、(2010年陕西中考)构建知识网络,可以帮助我们理解知识间的内在联系。右图是盐酸与不同类别物质之间反应的知识网络。
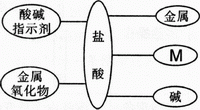 (1)图中M应为 ______ 类物质。
(1)图中M应为 ______ 类物质。
(2)写出一种能与盐酸反应的金属__。
(3)盐酸能与碱反应的实质是盐酸中的 H+ (写离子符号)与碱中的_______反应生成H2O。
(4)用盐酸除铁锈(主要成分Fe2O3)的化学方程式是 _________________。
【复习要点】2、酸的化学性质(通性)和用途
(1)酸具有通性的原因
酸溶液中都含有氢离子(或H+),因此酸具有相似的化学性质。
酸的通性
酸的化学性质 | 反应的化学方程式 | 实验现象 |
酸与指示剂的反应 | 酸使紫色石蕊溶液变___;使无色酚酞溶液____ | |
酸与活波金属的反应 | 镁与稀盐酸、稀硫酸 | 有______产生 |
锌与稀盐酸、稀硫酸 | 有______产生 | |
铁与稀盐酸、稀硫酸 | 有______产生,溶液由____色变为____色。 | |
酸与金属氧化物反应 | 氧化铁与稀盐酸、稀硫酸 | 红色粉末逐渐消失,溶液由____色变为____色。 |
氧化铜与稀盐酸、稀硫酸 | 黑色粉末逐渐消失,溶液由____色变为____色。 | |
酸与碱的反应 | 氢氧化钠与稀盐酸、稀硫酸 | 反应无现象 |
氢氧化钙与稀盐酸、稀硫酸 | ||
与盐的反应 | 碳酸钙、碳酸钠与稀盐酸 | 有______产生 |
硝酸银溶液和稀盐酸 氯化钡溶液与稀硫酸 | 生成______ |
(二)常见的碱
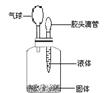 【回顾知识习题】例3、要使右图装置中的小气球鼓起来,实验时使用的固体和液体应该是( )
【回顾知识习题】例3、要使右图装置中的小气球鼓起来,实验时使用的固体和液体应该是( )
①镁和稀盐酸 ②石灰石和盐酸 ③氯化钠和水
④氢氧化钠和水⑤生石灰和水 ⑥硝酸铵和水
①②④⑤ B.①②③⑤
C.①②④⑥ D.①③④⑤
【复习要点】1、氢氧化钠、氢氧化钙的物理性质
氢氧化钠NaOH | 氢氧化钙Ca(OH)2 | |
俗称 | ||
色态 | 白色固体 | 白色固体 |
溶解性 | ___溶于水,并放出大量的___ | ___溶于水 |
特性 | 氢氧化钠固体易___________而潮解 | 溶解度随温度的____而__ |
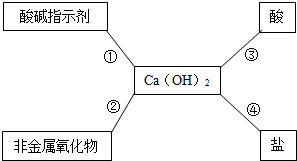 【回顾知识习题】例4、如图是有关氢氧化钙的知识网络。
【回顾知识习题】例4、如图是有关氢氧化钙的知识网络。
(1)遇氢氧化钙溶液变红的酸碱指示剂
是___________。
(2)若图中非金属氧化物为CO2,
则反应②的化学方程式___________。
(3)反应③在生产中的一种用途是______。
(4)有反应④制取NaOH所用到的盐是___,发生反应的化学方程式为________。
【复习要点】2、碱的化学性质
(1)碱具有通性的原因
碱溶液中都含有氢氧根离子(或OH-),所以它们具有相似的化学性质。
碱的化学性质(或通性)
碱的化学性质 | 反应的方程式 | 实验现象 |
碱与指示剂的反应 | 碱使紫色石蕊溶液变___; 使无色酚酞溶液____ | |
碱与非金属氧化物的反应 | 氢氧化钠溶液与二氧化碳 | 无现象 |
氢氧化钙溶液与二氧化碳 | 澄清石灰水变____。 | |
碱与酸的反应 | 氢氧化钠溶液与盐酸 | 无现象 |
碱与盐的反应 | 氢氧化钠溶液与硫酸铜溶液 | 产生_______ |
氢氧化钠溶液与氯化铁溶液 | 产生_______ | |
氢氧化钙溶液与碳酸钠溶液 | 产生_______ |
【命题点一】常见的酸
例1、(2015·湖北黄冈)构建模型和构建知识网络是化学学习中重要的学习方法,李华同学利用左手构建酸的性质知识网络,如图所示,请结合图示回答下列问题:
(1)如用湿润的pH试纸测定盐酸的pH,则结果会__________(填“偏大”“偏”或“无影响”)。
(2)图中①的现_______________________。
(3)写出一个符合图中③的化学方程式:_______________。
(4)图中性质④属于___反应(填基本反应类型)。
(5)图中⑤的性质在工业上可用于______(填用途)
【命题点二】 常见的碱
 例2、(2013年陕西)许多化学反应都伴随着明显的现象。但也有一些观察不到明显现象。请回答下列问题:
例2、(2013年陕西)许多化学反应都伴随着明显的现象。但也有一些观察不到明显现象。请回答下列问题:
向FeCl3溶液中滴加NaOH溶液,出现的明显现象_____。
(2)盐酸与NaOH溶液的中和反应也无明显现象,为证明二者确实发生了化学反应,在向NaOH溶液中滴加盐酸前,应先向NaOH溶液中滴入少许 _____________。
(3)CO2与NaOH溶液的反应无明显现象。为证明二者发生了反应,小红同学设计了如右图所示的实验。向一盛满CO2气体的锥形瓶中注入一定量的NaOH溶液,迅速塞紧橡皮塞(胶塞中插有一下端系小气球的玻璃管)。然后振荡锥形瓶,
会观察到小气球逐渐胀大,其主要原因是___________________________。
【知识拓展】 探究二氧化碳与氢氧化钠溶液反应
1、原理:CO2+2NaOH====Na2CO3+H2O
2、验证氢氧化钠是否和二氧化碳反应的思路
(1)可以利用密闭的装置,根据氢氧化钠和二氧化碳反应后会导致密闭容器中压强减小,从而引起现象的变化而判定。
思路判断时常出现的问题:氢氧化钠溶液中含有水,二氧化碳也能和水发生反应,必须设计对比实验排除水对实验结果的影响。
(2)可以利用反应后的产物为碳酸钠(同学们,请写出你的方法)
方法 | 现象 | 反应原理 |
例3、一次,小刚在实验室看到了右图情景:他首先想到药品可能变质了,那么NaOH溶液在空气中变质的化学方程式为________________;
小刚利用实验室的三种试剂(氯化钙溶液、稀盐酸、酚酞试剂)对这瓶“NaOH溶液”展开了探究。
[提出猜想]
猜想①:氢氧化钠溶液没有变质
猜想②:____________________
猜想③:氢氧化钠溶液完全变质
[实验探究]
方案 | 现象 | 结论 | |
1 | 取少量溶液于试管中,滴入足量_______试剂 | 产生大量气泡 | 猜想①不成 |
2 | 取少量溶液于试管中,滴加酚酞试剂 | 溶液变红 | 溶液中一定含有NaOH |
3 | a.取少量溶液于试管中,滴加足量_______试剂 | __________ | 猜想②成立 |
b.向a中所得溶液中滴加酚酞 | 溶液变红 | ||
经过思考,小刚否定了方案2的结论,理由是____________________。
[反思评价]氢氧化钠溶液暴露在空气中容易变质,故应____________保存。
作业布置:试题研究 满分特训方案 专题6 常见的酸和碱
课堂小结:同学们你的收获是什么?你还有什么困惑?
|
|
|
