任娟:淳化送教示范课交流案及说课稿,课题5-1质量守恒定律(第一课时)
课题5-1质量守恒定律(第一课时)
学 习 目 标 | 1、通过实验探究认识质量守恒定律以及守恒的原因 2、会利用质量守恒定律解释实验现象 3、从微观角度认识在一切化学反中,反应前后原子的种类和原子的数目没有增减。 | ||||||||||||||||||||||||||||||||||||||||||
学 习 过 程 | 一、实验探究 实验目的:探究反应前后物质的质量关系 实验内容:方案1- 红磷燃烧前后质量变化的测定 方案2- 铁钉与硫酸铜溶液的反应 完成下表
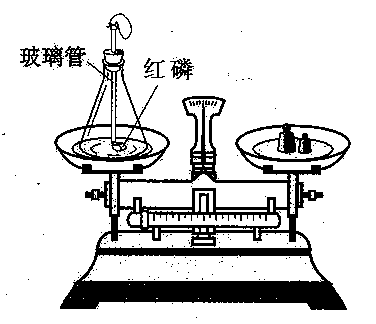
(1 写出红磷的燃烧文字表达式: (2)在红磷的燃烧实验中,气球为什么先变大,后收缩? (3)在红磷的燃烧实验中,气球的作用是什么?如果不要气球会有什么后果?
方案2思考题: (1 如果本实验前后均未塞胶塞,那么天平最终是否保持平衡?如果在方案1中去掉气球, 那么天平最终是否保持平衡? (2)反应体系是否密闭与测定结果有什么关系?(请同学们参考下面两个实验回答此题)
小结:无气体参加反应和生成时,天平始终平衡;有气体反应或生成的时候,天平不一定平衡,还要看体系是否密闭。 二、质量守恒定律: 1、内容:________________________________________________________________ ________________________________________________________________ 注意: ①“参加化学反应的各物质的质量总和”,没有参加反应的物质不包括在内; ②“生成的各物质的质量总和”,应当包括生成的各种物质,如沉淀、气体等。 列举有气体生成的反应: ③ 定律研究的仅是指“质量”,不能任意扩展到其它物理量; ④ 定律是一切化学反应都遵守的 ,但物理变化不属于此定律范畴; 2.从微观角度理解质量守恒定律成立的原因 在一切化学反应中,反应前后 没有改变, 没有增减, 也没有变化。 所以,化学反应前后各物质的质量总和必然相等。 3·从宏观和微观两方面认识质量守恒的本质。 【拓展提升】 1、推断反应物或生成物的组成元素 酒精在氧气中燃烧生成二氧化碳和水,能否根据这一事实,推断出酒精中肯定有______元素?可能会有________元素? 2、根据质量守恒定律,在X2+3Y2=2Z中,Z的化学式用X、Y表示应是 ( ) A、XY2 B、XY3 C、X2Y3 D、X3Y2 3、 “点石成金”可能吗?水能变成汽油吗? | ||||||||||||||||||||||||||||||||||||||||||
【课堂 堂 检 检测 | 1、解释反应前后物质的质量变化 (1)根据质量守恒定律解释细铁丝在氧气中燃烧后,生成物的质量比细铁丝的质量大。 (2)高锰酸钾受热分解后,剩余固体的质量比原反应物的质量小,因此这个反应不遵守质量守恒定律。你认可这种说法吗?为什么? 2、 用质量差确定某反应物或生成物的质量 在A+B=C+D的反应中,5克A跟一定量的B恰好完全反应,生成3克C和10克D,则B的质量_____克。 3、判断下列题,正确的打“√”,错误的打“×”。 ⑴ 水冷却结成冰,总质量没有改变 ,由此说明:此变化符合质量守恒定律。 ( ) ⑵ 参加反应的氢气和氧气的体积一定等于生成水的体积 ( ) 4、化学反应前后: ①物质的化学性质 ② 原子的种类 ③元素的种类 ④分子的数目 ⑤反应物质量总和与生成物质量总和. 其中一定不发生变化的是 ( ) A. ①②③④⑤ B. ①②③⑤ C. ②③⑤ D. ①③④ 5、某物质在干燥的空气中燃烧后的产物是一氧化碳、二氧化碳和水,由此推断,该物质的组成中一定含有的元素是( ) A.碳、氢元素 B.碳、氧元素 C.氧、氢元素 D.碳、氧、氢元素 【小结】你学会了什么? |
《质量守恒定律》说课稿
一·说教材
本节课是义务教育课程标准人教版化学实验教科书九年级上册第五单元课题1《质量守恒定律》,包括质量守恒定律的含义、质量守恒的原因及其应用。
1、教材的地位和作用
质量守恒定律是初中化学的一个重要化学规律,是分析物质在化学反应中的质量关系的理论依据,它的应用贯穿于整个中学化学。本节教材在初中化学里有着承上启下的作用。在此之前,学生学习了元素符号、化学式、分子和原子的初步知识,对化学反应中物质发生了质的变化已经有了一定的认识。本节课的教学将引领学生对化学反应的认识开始了从“质”到“量”的过渡,也为之后化学方程式的书写和计算的教学构建了理论铺垫,所以本课内容不仅是本单元的一个重点,也是整个中学化学的教学重点之一。
2、教学目标
根据新课标的精神、教材的编写意图、学生的认知水平、心理特点,确定本节课的教学目标为:
(1)知识与技能:
①理解质量守恒定律以及守恒的原因,
②学会运用质量守恒定律解释和解决一些问题。
(2)过程与方法:
①通过实验探究,增强发现问题、探究问题的能力。
②通过对质量守恒原因的分析,培养逻辑推理能力,学习研究化学问题的基本思路。
(3)情感、态度、价值观:
①培养学生善于合作、勇于探索的科学精神。② 培养定量分析观点
3、教学重点:理解质量守恒定律的涵义
教学难点:理解质量守恒的原因,从而达到从定量角度理解化学反应。
二·说教法
学生的化学知识和对于化学探究学习方法的了解都属于启蒙阶段,若探究过程不符合学生现有的认知水平和心理特点,过于放开或加大难度,不仅不能收到理想的探究效果,而且会挫伤学生参与探究性学习的积极性。因此本节课我采用的是情景问题法及教师引导下的学生自主探究法和交流讨论法。
1·在引课时采用情景问题法
教师设置情境,提出问题引导学生真正成为主动的探究者。
2·在探究质量守恒定律时用实验探究教学法 :
我将本班学生分成A、B、 C三个大组分别探究教材的三个实验。既培养了学生的科学探究能力,也培养了学生的合作精神、把教与学统一起来。
3·质量守恒定律的微观解释用多媒体展示法。
运用Flash动画进行微观演示,帮助学生从微观上理解质量守恒定律。
三·说学情分析
已了解了元素符号、化学式、化学反应的实质,初步掌握了一些简单的化学反应。初步掌握了简单的化学实验基本操作技能,而对化学探究学习方法的了解尚处于启蒙阶段。学生刚开始化学学习,情绪和心理都处于比较兴奋、好奇状态。
四、 说学法
交流案引领学生进行自主探究,教师启发学生思考、讨论、归纳、实验探究法、等多种方法相结合。让在课堂上既有师生交流又有生生交流。
五·说教学过程
(一)创设情景——问题引课
(展示前面所学化学变化图片)我们知道反应物之间发生化学反应可以生成新物质,但在这些反应中反应前后各物质的质量总和有什么变化?
(二)实验探究——合作学习
采用分组探究实验组织教学。
1.确定探究内容(教材92—94页)
A组:探究白磷在空气中燃烧前后质量变化情况
B组:探究铁钉和硫酸铜溶液反应前后质量变化情况
C组:探究盐酸与碳酸钠反应前后质量变化情况
2.实验仪器和药品:
A组:天平、250mL锥形瓶、酒精灯、镊子、沙子、切好的白磷、气球。
B组:天平、250mL烧杯、铁钉、硫酸铜溶液、
C组:天平、250mL烧杯、盐酸、碳酸钠粉末、小针筒、锥形瓶。
3.分组实验、观察现象
根据探究步骤进行实验, A、B两组都得出:反应前后质量不变。分析C组缘故。
4·归纳结论
质量守恒定律:参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。
理解质量守恒定律注意的问题:
1)“守恒”指的是质量守恒,其它方面如:体积不一定守恒;
2)“参加反应的各物质”,不包括没有参加反应的物质在内;
3)“生成的各物质的质量总和”,应当包括生成的各物质,如:沉淀、气体等。
4)质量守恒定律仅用于化学变化。
通过刚才三个探究实验的共同结果是——反应前后质量不变。提出“为什么?”,这是学生理解的难点。
(三)动画教学——突破难点
利用动画模拟白磷在空气中燃烧、水的电解等微观过程,直观形象地说明质量守恒的原因。实现思维的碰撞、思想的启迪。总结为三个不变。
(四)课堂练习——学以致用
做好课堂同步练习,提高应用知识的能力。
(五)课堂小结
通过本课题的学习,你获得了哪些知识和学习方法?
【学生自由发言,相互补充,总结出本课知识框架,理清学习思路,教师适当的评价鼓励,帮助学生肯定自我,欣赏同学。】
(六)课后作业
课本98页,习题第3、4题。
六·板书设计
规范的板书有利于学生对知识的系统理解,使学生对本堂课的知识有个完整的印象,因此本节内容的板书采用框架式,让学生更直观形象的理解质量守恒定律,并加深其记忆。
七、教学反思:
质量守恒定律是初中化学中的重要定律,抓住三点。第一点要重视实验。从反应验前物质的质量关系出发,通过探究,思考去“发现”质量守恒定律,而不是去死记硬背定律。第二点正确理解质量守恒定律。强调“参加反应的各物质”“反应后生成的各物质”“质量总和”。第三点从本质上理解质量守恒定律。之所以化学反应前后各物质的质量总和必然相等,是因为在一切化学反应中,反应前后原子的种类没变,原子的数目没变,原子的质量没变。化学反应的实质就是参加反应的各物质的原子重新组合而生成其它物质(生成物)的过程。
教学亮点
1· 体现学生自主探究与合作交流的学习方式。
2·以小组为单位,以“交流案”为依托,构建探究交流氛围。
3.体现“宏观—微观”的思想,彰显学科特征。
|
|
|