霍雅静:第四单元 生命之源—水复习课交流案
教学目标: 1、知道水的物理性质,认识水的组成;
2、了解水污染及防治;了解水的净化及纯化;知道硬水和软水。
3、认识质量守恒定律,能解决相关问题。
4、能正确书写常见的化学方程式;学会根据化学方程式进行简单计算。
教学重点:水污染、净化、硬水与软水;质量守恒定律;化学方程式书写及计算
教学难点:质量守恒定律;化学方程式书写与计算
教学方法:自主复习;小组互助;点拨归纳
教学过程:
【问题驱动,自主复习】
认识水资源
水的污染与防治 人们在利用水时,导致了水源的污染,其污染源主要是 、 、 。从以上三方面提出防治水污染的措施有 、 、 。
水的组成 探究水的组成是根据 实验得出的。
(在通电前,先向蒸馏水中加入少量的 ,目的是 。
(实验现象:通电后,两极上 ,一段时间后,与电源 相连的试管中产生的气体体积大约是与电源 相连的试管中产生气体的体积的两倍,其质量之比为 。
(检验与电源正极相连的试管中产生的气体的方法是 ,出现木条 现象,证明产生了 ;检验另一试管中产生的气体的方法是 ,现象是 ,证明产生了 。
(实验结论:
①从宏观看:氢气是由 组成的,氧气是由 组成的,因此水是由 组成的。
②根据“同温同压下同体积气体分子数相同”的规律,由于电解水产生的氢气和氧气的体积比为 ,故其分子数之比应为 ,又由于氢分子和氧分子都是 原子分子,它们都来自于水,所以可推知水的化学式为 。
③从化学反应的实质看:水 分解成 原子和 原子,氢原子构成氢 ,氧原子构成氧 ,大量的氧 聚集成氧气,氢 聚集成氢气。
④分子和原子的根本区别是 。
水的软化和净化 (1)净化水的方法有沉淀、过滤、吸附和蒸馏等。其中过滤法可除去水中 杂质;活性炭的作用是 。净化程度最高的是 。
(证明水是否纯净,可以用 法。此时用到的主要玻璃仪器有 ,此操作过程中玻璃棒的作用是 。
(蒸馏得到的水是 ,但不宜长期饮用,因为里面不含有益于人体健康的微量元素。硬水是指 的水,硬水有很多危害:会使锅炉 ,洗衣服会 。软水是指 的水。将硬水软化的方法,在工业上常用 法,在家中常用 法。区别硬水和软水常用 ,根据 的现象来区分。
2 质量守恒定律
(质量守恒定律的概念 质量守恒定律是指在化学反应中, 质量总和等于 质量总和。
(质量守恒定律的理解
①适用范围:只适用于一切 而不包括 。
②“参加反应”的含义:不是反应物质量的简单相加,没参加反应的物质质量 计算在内。还应包括参加反应的 的质量。
③“反应后生成”的含义:指新产生的物质的质量,包括产生的气体和沉淀的质量。原有的质量 能计入质量总和中。
④“质量总和”的含义:不能漏掉任何一种状态的物质,包括 和 的质量。
⑤“质量守恒”的含义:只指物质的 ,物质的体积、密度、分子数等不一定守恒。
(质量守恒定律的微观解释 化学反应的过程,从微观看就是 的过程。也就是在化学反应前后 没有发生变化。
(从质量守恒定律理解化学反应的特点 六不变: 、 、 、
、 、 ;两改变 、 ;两个可能变 、 。
三、化学方程式
1、化学方程式的定义 指用 来表示 的式子。
2、化学方程式的意义 化学方程式可表示 、 和 ,从微观表示微粒之间的 关系;还可表示反应物和生成物各物质之间的 关系。由此化学方程式的读法为:以C+O2= ==CO2为例,宏观可读作 ,从量的角度可读作 ;微观可读作 。
3、化学方程式的书写
书写化学方程式必须遵循两个原则:① ② 。
4、根据化学方程式计算 化学方程式表示各物质质量关系是通过相对分子质量与化学计量数的乘积表示出来的,且计算时都必须是纯净物的质量。计算步骤为:① :不带单位,有具体物理量(如质量、体积);②写出完整正确的 。(化学式和配平是重点);③写相对质量并标明已知量和未知量:已知量带单位,未知量不带单位;(已知量必须是纯净物质量)④ :横向列比例,已知量带单位,未知量不带单位;⑤ :结果带单位;⑥ 。
【展示分享,点拨归纳】
1、小组交流复习成果,解决复习中存在的问题。
2、重难点突破。
(1)质量守恒定律的理解及应用
(2)化学方程式书写
(3)化学方程式计算
【典例分析,拓展提高】
1.煤气中添加少量有特殊臭味的乙硫醇(C2H5SH),可以提醒人们预防煤气泄露。乙硫醇在煤气燃烧过程中也可充分燃烧,其反应方程式为2C2H5SH + 9O2 点燃 4CO2 + 2X + 6H20, 则 X 的化学式为: ( ) A.SO3 B.SO2 C.CO D.H2SO4
2.在反应A+B=C+D中,20gA和10gB恰好完全反应,生成5 gC。若要制得5gD,则需要B的质量为( )A.5g B.4g C.2g D.3g
3.一个密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得数据见下表。下列说法中正确的是 ( )
物质 | 甲 | 乙 | 丙 | 丁 |
反应前质量 | 8g | 35g | 5g | 8g |
反应后质量 | 2g | X | 5g | 42g |
A.X=7g B.在该反应中,丙物质一定做催化剂 C.该反应是分解反应
D.在该反应的化学方程式中,甲、丁的化学计量数之比为1∶l
4.配平下列方程式:
(1) Al+ H2SO4------ Al2(SO4)3+ H2
(2) CO+ Fe2O3-------- Fe+ CO2
(3) C2H5OH+ O2-------- CO2+ H2O
(4) CO+ NO---------- N2+ CO2
5.乙醇是一种清洁燃料,但在氧气不足时燃烧,会生成一氧化碳。现有207g乙醇与一定量的氧气点燃后发生如下反应:3C2H5OH+8O2====xCO2+2CO+9H2O。
(1)根据质量守恒定律可知:x=
(2)计算该反应生成一氧化碳的质量。
【变式训练,强化能力】
1、如图是“尾气催化转化器”将汽车尾气中的有毒气体转变为无毒气体的微观示意图,其中不同的圆球代表不同的原子。下列说法错误的是( )
A.此反应有单质生成 B、原子在化学变化中是不可分的
C、图中的反应物全部是化合物 D、参加反应的两种分子的个数比为2:3
催化剂
2、在A+3B=2C+2D的反应中,14gA完全反应后生成44gC和18gD,若A的相对分子质量为28,则B的相对分子质量为( ) A.16 B.32 C.64 d 96
3、在实验室里加热30g氯酸钾和二氧化锰的混合物制取氧气,完全反应后剩余固体质量为20.4 g。请计算:
(1)生成氧气的质量为 g。
(2)原混合物中氯酸钾的质量。
【当堂检测,总结提升】
1.写出下列反应的化学方程式,并在括号内注明反应的基本类型:
①碳在氧气中燃烧 ②过氧化氢在二氧化锰催化下分解
_________________________( ) _______________________________( )
③红磷在空气中燃烧 ④ 氯酸钾与二氧化锰混合共热
_________________________( ) _______________________________( )
⑤铁丝在氧气中燃烧 ⑥镁条燃烧
__________________________( ) _______________________________( )
⑦加热高锰酸钾制取氧气 ⑧水通电分解成氢气和氧气;
____________________________( ) __________________________( )
2、物质发生化学变化的前后,总质量是否发生改变?是增加、减小还是不变?小刘、小李按下面的步骤进行探究:
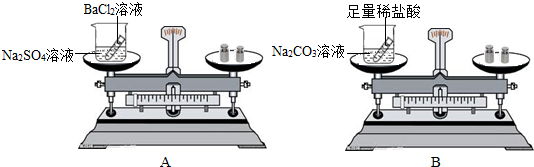
(1)提出假设:物质发生化学变化前后总质量不变.
(2)设计并进行实验:小刘设计的实验装置和选用药品如A所示,小李设计的实验装置和选用药品如B所示,他们在反应前后都进行了规范的操作、准确的称量和细致的观察.
①这两个实验所发生的化学反应方程式为:
小刘的实验:Na2SO4+BaCl2=BaSO4↓+2NaCl 小李的实验:Na2CO3+2HCl=2NaCl+CO2↑+H2O
②实验结论:
小刘认为:在化学反应中,生成物的总质量与反应物的总质量相等;
小李认为:在化学反应中,生成物总质量与反应物总质量不相等.
③你认为 的结论正确,导致另一个实验结论错误的原因是: 。
请你谈谈对另一个实验的改进方法: 。
④请从原子的角度分析你认为正确的结论的原因: 。
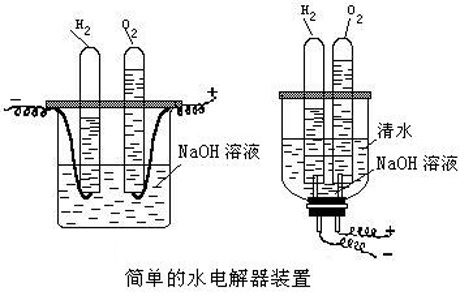 3. 水是人类最宝贵的自然资源,多一滴水就可能多一条生命。小明利用下图所示装置探究水的组成。
3. 水是人类最宝贵的自然资源,多一滴水就可能多一条生命。小明利用下图所示装置探究水的组成。
(1)通电一段时间后,试管a与试管b所收集到的气体的体积之 比为 。该实验得到的结论是 (只写一条)。
(该反应的化学方程式为 。
(3在自来水厂里,水的净化过程主要包括絮凝、过滤、曝气、杀菌。经过这样处理
所得的水是 (选填“纯净物”或“混合物”)。
(假如你是一名水质检验员,用简单的方法检验水样是硬水还是软水,可以加入 搅拌,看其产生泡沫的多少。若检验时发现水硬度较高,你建议在饮用前可采取的处理办法是 。
(5)家庭净水器中含有大量的活性炭,活性炭起 作用。
4、某干燥剂含氧化钙的质量分数是80%(杂质不吸水),理论上14g干燥剂能吸收水的质量是多少?(CaO+H2O==Ca(OH)2)