霍雅静:第二章 空气 物质的构成复习交流案
教学目标:1、知道空气各成分,掌握氧气含量测定方法,了解氮气和稀有气体的性质和用途。
2、能够正确区分物质的种类。
3、掌握分子、原子、离子与物质之间的关系,知道原子的内部结构及离子的形成过程。
4、通过对空气污染与防治的学习,激发学生爱护环境的意识。
教学重点:分子、原子和离子的区分;物质种类的区分;空气中氧气含量测定。
教学难点:分子与原子的区别;物质种类的区分。
教学方法:
教学过程:
【问题驱动,自主复习】
一、空气的成分及其污染
(1)空气的成分 空气按体积分数计算,其含量最多的为 ,约占 ,其次是 ,约占 , 约占0.94%,二氧化碳约占 ,其他气体和杂质约占 .
(2)空气中氧气含量测定 如图是常见的测定空气成分的实验装置:
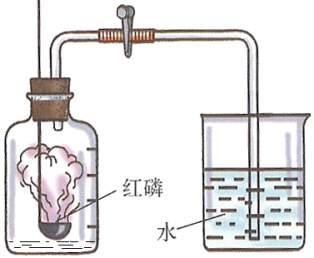 实验原理是
实验原理是
所用药品为 ,且用量应 。其反应的文字表达
式为
实验现象: ,待冷却后打开止水夹进入容器内水的体积约占气体体积的 。
实验的结论是 ,通过实验还可知道氮气的性质有 。
误差分析 实验中若测定的结果小于1/5,可能原因是:a ;b ;c ;若结果大于1/5,其可能的原因是 ; 。
实验拓展 该实验不能用木炭代替红磷的原因是 ;也不能用铁丝代替是因为 ;镁条也不能用来完成实验是因为镁与氧气、氮气、二氧化碳均能反应。
(3)空气污染及防治 空气污染的污染源主要有工业污染、交通污染和生活污染,其产生的污染物主要分为气体污染物和颗粒状污染物,气体污染物主要有 、 和 。
其中能引起酸雨的是 ,二氧化碳所产生的环境问题是 。请写出三条防治空气污染源的措施: 。
2、氮气和稀有气体的用途
氮气在常温下化学性质稳定,可用做 ;在高温高能量下反应可用来生产
;稀有气体化学性质稳定,可用作 ,在通电时能发出不同颜色的光,可用于 ,由于 密度非常小,且稳定,可用于填充 。
3、构成物质的微粒
分子、原子的特性 ①都是在 ;②微粒之间有 ;③微粒的
和 都很小。湿衣服很快就能晾干,说明 ;物体都有热胀冷缩现象是因为微粒之间有 。
分子及其性质 分子是构成物质的一种微粒,由分子构成的物质,在物理变化中,分子本身 ,在化学变化中,分子本身 ,生成 。新分子与原分子化学性质 。说明分子是保持物质 的一种微粒。固体碘和碘蒸气均能使淀粉变蓝,说明同种分子性质 。双氧水能杀菌,但水不能是因为构成它们的 不同,所以化学性质不同。
原子及其构成 原子也是构成物质的一种微粒,由原子直接构成的物质有 、 、 。分子也是由原子构成的。原子是化学变化中的最小微粒。分子和原子的本质区别是在化学变化中 可分而 不可分。
化学变化的实质是分子 成 ,原子重新组合成新 ,构成新物质。
原子是由 和核外 构成的,原子核是由 和 构成的。质子带 电,电子带 电,中子不带电。核内质子数 核外电子数 核电荷数。原子的质量很小,在计算时通常用其相对原子质量。某原子的相对原子质量等于
。由此可见,相对原子质量是一个比值,其单位是 。相对原子质量约等于 和 之和。
离子及离子结构 离子也是构成物质的一种微粒。如 是由离子构成的。离子是带电的 或 。离子可分为 和 。
氯元素原子的结构示意图为 ,其核电荷数为 ,核外有 个电子层。最外层上有 个电子,在化学反应中易 电子,形成带 电的 离子。
金属元素的最外层电子数目一般 4个,在化学反应中易 电子形成带正电的 离子。
稀有气体元素的原子最外电子层一般有 个电子,其中氦有 个电子。因此它们的化学性质比较 。
原子和它形成的离子质子数相同,电子数不同,所以其质量相同。
与氖原子电子排布相同的离子有 、 、 、 、 、 。
4、元素
元素是指具有相同 或 的同一类原子的总称。元素是宏观概念,只讲种类不讲个数。而原子是微观粒子,既讲种类又讲个数。地壳中含量前四位的元素 、 、 、 。
元素符号的意义:H:既表示氢元素,又表示 。前面加数字表示几个原子,不再表示元素。如3H表示 。由原子直接构成的物质还可表示该物质。如Fe表示铁这种物质。
5、物质的分类
纯净物是由 组成,混合物是由 组成。如果物质是由分子构成的,则纯净物中只有 种分子,混合物中有 种分子,所以纯净物有固定的组成,可用化式表示。混合物中各组分保持原有的化学性质。纯净物可分为 和 。单质是由同种 组成的 。化合物是由 种元素组成的 。化合物中有一类氧化物是由 元素组成且其中一种为 的化合物。因此同种元素组成的物质不一定是单质,如氧气与臭氧的混合物。
【展示分享,点拨归纳】
1、小组交流复习成果,解决复习中存在的问题。
2、重难点突破。
(1)物质类别的判断及分类标准
(2)分子、原子、离子所构成物质的判断
(3)原子、离子结构示意图的判断及符号表示
(4)从微观角度解释某些现象
【典例分析,拓展提高】
1、在下列几种物质中属于混合物的是 ;属于纯净物的是 ;属于单质的是 ;属于化合物的是 ;属于氧化物的是 ;属于金属单质的是 ;属于非金属单质的是 。
①氯化钠 ② 氢氧化钠 ③四氧化三铁 ④液氧 ⑤水银
⑥空气 ⑦食盐水 ⑧红磷 ⑨硫粉 ⑩铁粉
2、下列现象说明了什么?用分子、原子的观点解释
①“南国汤沟酒,开坛十里香”
②体温计测体温时汞柱上升。
③液氧和氧气都能支持燃烧。
④双氧水和水的化学性质不同。
⑤水在通电情况下分解成氢气和氧气。
3、下列四种粒子的结构示意图中,说法正确的是( )

① ② ③ ④
A.它们表示四种不同的元素 B.③④表示的两种粒子化学性质相似
C.①③④表示的元素都是非金属元素 D.①④表示的是阳离子
【变式训练,强化能力】
1、下列各图中两个符号分别表示两种不同的原子,其中能表示由两种化合物组成的混合物的图是( )
A B C D
2、从微粒的角度解释以下现象
①一滴水中约有15亿个水分子
②皮球内充满气体容易压瘪。
③预防流感时,常采用给醋加热法。
④酒精挥发和酒精燃烧本质是否相同?
⑤一氧化碳与二氧化碳具有不同的化学性质。
3、下图中的①、②是氟元素、钙元素在元素周期表中的信息,A.B.C.D是四种粒子的结构示意图。请你回答:
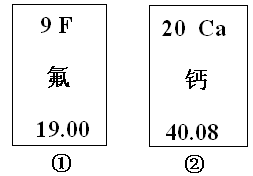
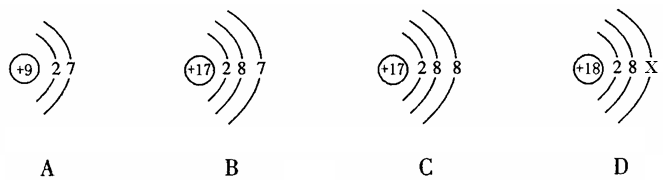
(1)氟元素的相对原子质量为 ,钙元素的原子序数为 ;(2) D中的X= ;
(3) C的粒子符号是 ;
(4)A粒子的化学性质与B.C.D中哪一种粒子的化学性质相似 (填序号);
(5)B和______属于同种元素的粒子(用“A”、“C”、“D”填空)。
(6)以上A、B、C、D粒子结构示意图中,表示稀有气体元素的原子的是________;
【当堂检测,总结提升】
1、将下列物质的序号填入物质所属类别的空格内
①空气 ②海水 ③液态氧 ④二氧化碳 ⑤高锰酸钾⑥冰水共存物 ⑦水银 ⑧氯化钾 ⑨5%的过氧化氢溶液 ⑩四氧化三铁
⑴混合物_____________________ ⑵纯净物_____________________
⑶化合物_____________________ ⑷氧化物_____________________
⑸单质________________________
2、对于Fe、Fe2+、Fe3+三种粒子的判断,正确的是( )
①核电荷数相同②核外电子数相等③电子层结构相同④质量几乎相等⑤等质量的三种粒子所含质子数相等
A、①④⑤ B、①③⑤ C、②③④ D、①②③④⑤
3、用微粒观点解释下列问题:
(1)保持氧气化学性质的微粒是 。
(2)二氧化碳是由 构成的。
(3)水通电分解过程中,不变的微粒是 。
(4)用湿抹布擦过的桌面,一段时间后变干的原因是 。
(5)一定质量的干冰升华,其体积变大的原因是 。
4、从下列粒子的结构示意图中,写出该示意图的符号
5、下列符号中既能表示一种元素又能表示一种原子,还能表示该物质的是( )
A、2N B、N C、C D、N2