于海玲工作室初中化学公益微课堂-于海玲微课复习过氧化氢制取氧气的方法
于海玲微课“复习过氧化氢制取氧气的方法”
![]()
课 题:复习过氧化氢制取氧气的方法
一级主题:身边的化学物质
二级主题:空气氧气
内容简介:本节课通过用过氧化氢制取氧气反应原理的分析,实验装置的选择、组装,及制备氧气实验视频的回放,加深对用过氧化氢制取氧气方法的复习。同时,通过练习,进一步强化有关实验操作要点和注意事项。
授课教师:于海玲
课后练习:
1、用双氧水制氧气时,忘了加二氧化锰,其结果是 ( )
A.不放出氧气 B.放出氧气的速度慢
C.放出氧气的总量少 D.放出氧气总量减少且速度减慢
2、下图是实验室制备气体的常用装置,请回答下列问题。
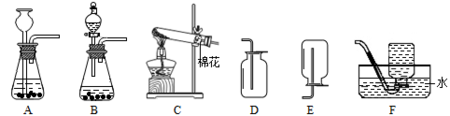
(1)A装置中长颈漏斗必须伸入液面以下的原因是________________________。
(2)请从上述装置中选出实验室用过氧化氢溶液和二氧化锰制取氧气的一组发生和收集装置_____(填字母),该反应的化学方程式是__________________,MnO2起_________作用。
(3)用装置_____(填字母)收集的气体较纯或无需验满,若用该装置收集的氧气不纯,则可能的原因是__________________(答出一种即可)。
(4)用A或B装置制备气体的反应应该是________和液体不需要加热的反应。
(5)若用图G装置收集氧气,气体应从________ (填“a”或“b”)端进入。
(6)某同学将A装置进行了改进,如右图 I 装置、Ⅱ装置,其优点是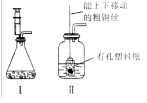 ___________________________(写一条即可)。
___________________________(写一条即可)。
3、科学探究是奇妙的过程,请你一起参与实验探究,并填写下列空白。
(1)[提出问题] 小华同学在滴加FeCl3 溶液时,不小心把滴加FeCl3 溶液的滴管放入到盛“双氧水”(过氧化氢)的试剂瓶中,发现有大量的气泡产生。小华联想到用二氧化锰可作过氧化氢分解的催化剂,他想FeCl3 溶液能否也可以作过氧化氢分解的催化剂呢?于是他做了以下探究。
(2)[猜想与假设] FeCl3 溶液能作过氧化氢分解的催化剂。
(3)[设计与实验]
实验步骤 | 实验现象 | 实验结论 |
在一支试管中加入5ml 15%的H2O2溶液,然后滴入适量的FeCl3溶液,把带火星的木条伸入试管。 | FeCl3溶液可以催化分解H2O2 |
(4)[讨论与反思]
已知FeCl3溶液中含有H2O、Fe3+和Cl-三种微粒,小森同学又做了三种猜想:
猜想1:真正催化分解H2O2的是FeCl3溶液中的H2O
猜想2:真正催化分解H2O2的是FeCl3溶液中的Fe3+
猜想3:真正催化分解H2O2的是FeCl3溶液中的Cl-
你认为最不可能的是那一种猜想 ,理由是
小华同学又对余下的两种猜想,进行了实验探究,请你帮助他填写下表:
实验步骤 | 实验现象 | 实验结论 |
向盛有5ml 15%的H2O2溶液的试管中加入少量的HCl,然后把带火星的木条伸入试管中。 | 无明显现象 | |
向盛有5ml 15%的H2O2溶液的试管中加入少量的 ,然后把带火星的木条伸入试管中。 |
参考答案
1、
B
2、(1)防止气体从长颈漏斗逸出
(2)AD或AF或BD或BF,2H2O2 2H2O+O2↑,催化作用
(3)F, 一开始有气泡产生时就开始收集(或装置漏气)
(4)固体
(5)a
(6)便于控制反应速率、便于反应随时开始和停止(其他合理答案均可)
3、带火星的木条复燃,1,H2O2溶液中就有水,Cl- 不能催化分解H2O2,Fe2(SO4)3, 带火星的木条复燃,Fe3+可以催化分解H2O2。
|
|
|
