4.3 质量守恒定律
年级:九年级 课型:新课 课时:1课时 审核:化学备课组
执笔:强锋妮 班级: 姓名: 时间:2015-11-26
【学习目标】
1.理解质量守恒定律的含义;2.通过对化学变化实质的分析,从微观角度认识质量守恒定律的本质;3.学会运用质量守恒定律解释一些现象。
【重点】理解质量守恒定律的含义及本质。
【难点】运用质量守恒定律解释一些现象。
【教学过程】
一、自主学习
化学变化的实质就是 的过程。如:给水通电,水分子先分解成了 和 ,然后这些原子重新组合成了 分子 和 分子 ,大量的分子聚集在一起形成了 和 。在这个过程中,氢原子和氧原子的种类、数目、质量都 (有或没有)发生变化。因此,被分解水的质量 (等于或不等于)生成的氢气与氧气的质量总和。
二、合作探究
(一)化学反应前后物质总质量的测定:
[提出问题]化学变化前后,反应前物质总质量与反应后物质总质量是什么关系?
[你的猜想] 。
[实验探究] 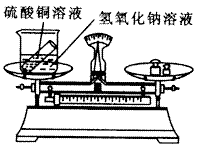 氢氧化钠溶液与硫酸铜溶液反应前后质量的测定。
氢氧化钠溶液与硫酸铜溶液反应前后质量的测定。
实验步骤:
(1)在烧杯中放入蓝色硫酸铜溶液,小试管中放入氢氧化钠溶液,称量反应前物质的总质量m1 = g;
(2)倾斜烧杯,使二者反应,观察现象;
(3)称量反应后物质的总质量m2 = g,并与反应前物质的总质量m1作比较。
[实验现象] 。
[实验结论]反应前物质总质量m1 反应后物质总质量m2
归纳总结: 叫做质量守恒定律。
(二)理解质量守恒定律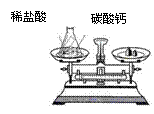
【讨论1】碳酸钙与稀盐酸反应后,质量减小,这违反质量守恒定律吗?为什么?
如何改进实验装置?改进之后的实验结论是: 。
归纳总结:若选择有气体参加或有气体生成的化学反应来证明质量守恒定律,
则反应一定要在 容器内进行。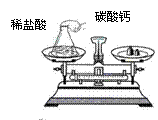
【讨论2】分析以下四个问题,总结出质量守恒定律中的关键词。
1.10g水受热变成10g水蒸气,符合质量守恒定律吗?为什么?
2.根据质量守恒定律推知,20ml氢气和10ml氧气充分反应能生成30ml的水,这句话对吗?为什么?
3.镁条在空气中燃烧,生成物的质量比镁的质量增加了,为什么?
4.已知12g碳与32g氧气恰好完全反应可生成44g二氧化碳,现在有12g碳与64g氧气,若充分反应,可以生成 g二氧化碳。
(三)质量守恒定律的原因(本质)
原子
化学反应前后 原子 不变 化学反应前后物质总质量不变
原子
三、小结
四、达标练习(完成课本第114页4.3习题中第4、8题。)
教(学)后反思: